Autores:pppp Paulo Cesar Naoum Paulo Francisco Naoum Cristiane Gutierres Toledo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Há
cerca de 800 tipos diferentes de hemoglobinas variantes descritas
na literatura científica. Desse total, cerca de 200 são
Hb Instáveis e que serão abordadas numa página
específica deste site (capítulo 8 – Hb Instáveis);
aproximadamente 50 variantes têm atividades funcionais específicas,
ex.: metaemoglobinemia por Hb M, Hb variantes com afinidade aumentada
ou diminuída pelo oxigênio, etc.; e cerca de 500 variantes
sem alterações fisiopatológicas (excetuando
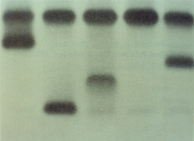
as Hb S e Hb C) importantes, ex.: Hb D, Hb J, Hb N, Hb O Anab, etc. Para que seja possível fazer uma consulta rápida a algum tipo de Hb variante de interesse do leitor nós propomos fazer uma abordagem referencial, baseada na sua posição eletroforética, usando eletroforese alcalina (pH 8 – 9) em meios de acetato de celulose ou em gel de agarose. Assim, consideraremos sete posições padrões em eletroforese alcalina para efeito agrupamos cerca de 100 Hb variantes: Hb A (padrão normal), Hb Fetal, Hb S, Hb C (todas mais lentas que a Hb A) e Hb K, Hb J e Hb I (ambas mais rápidas que a Hb A) conforme mostra a figura 5.9. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
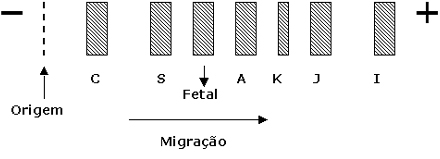
Figura 5.9 – Posições padrões de Hb A em relação às hemoglobinas Fetal, S e C (lentas) e J e I (rápidas). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
As Hb variantes causadas por mutações em globinas alfa e beta, descritas com maior freqüência na literatura, serão agrupadas conforme suas similaridades nas sete posições padrões da figura 5.9. As mutantes de globinas delta e gama serão apresentadas posteriormente. Para cada grupo descrito será indicado: · Mutação de aminoácido(s) na globina · Posição na eletroforese em agar-ácido (pH 5 a 6) · Eritrograma · Teste(s) específico(s) de rotina analítica · Características da hemoglobina As descrições serão iniciadas pelo grupo de variantes similares à Hb A, seguido na seqüência das lentas (Fetal, S e C) e das rápidas (K, J e I).
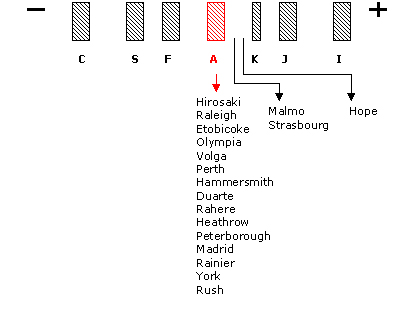
Essas variantes se devem a mutações que ocorrem geralmente na superfície interna da molécula, nos contatos a1b1 e a2b2 que dão estabilidade e nos contatos a1b2 e a2b1 responsáveis pela movimentação molecular durante a oxigenação. Por essas razões a maioria das trocas de aminoácidos envolvem os dos tipos hidrofóbicos (ver tabela 3.2) e com pI muito próximos. Assim, essas mutações não alteram a mobilidade eletroforética alcalina, mas podem causar hemoglobinas instáveis ou hemoglobinas com problemas na afinidade pelo oxigênio. A figura abaixo destaca as principais Hb variantes e suas posições similares ou próximas da Hb A que serão descritas. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hb Hirosaki (a 47 Fen – Leu) Eletrof. ágar-ácido: similar à Hb A Eritrograma: anemia hemolítica Teste específico: Pesquisa de Heinz: + e Instabilidade: + Característica: Hb Instável Hb Raleigh (b1 Val
– Ala) Hb Etobicoke (a 84
Ser – Arg) Hb Olympia (b 20 Val
– Met) Hb Volga (b 27 Ala
– Asp) Hb Perth (b 32 Leu
– Pro) Eletrof. ágar-ácido: similar à Hb A Eritrograma: anemia hemolítica Teste específico: Pesquisa de Heinz: + e Instabilidade: + Característica: Hb instável com cianose Hb Duarte (b 62 Ala
– Pro) Eletrof. ágar-ácido: similar à Hb Fetal Eritrograma: eritrocitose Teste específico: afinidade aumentada ao O2 Característica: Hb com alteração funcional Hb Heathrow (b 103
Fen – Leu) Hb Peterborough (b
111 Val – Fen) Hb Madrid (b 115 Ala
– Pro) Hb Rainier (b 145
Tir – Cis) Hb York (b 146 His
– Pro) Hb Rush (b 101 Glu
– Gln) Eletrof. ágar-ácido: entre Hb A e Hb Fetal Eritrograma: eritrocitose Teste específico: afinidade aumentada ao O2 Característica: Hb com alteração funcional Obs.: ver figuras 5.10 e 5.11 Hb Strasbourg (b 23
Val – Asp) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
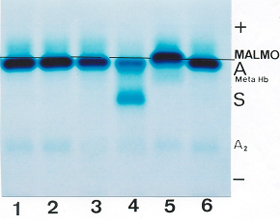
Figura 5.10 – Eletroforese alcalina em acetato de celulose mostrando a posição eletroforética de Hb Malmo discretamente mais rápida que a Hb A. O risco traçado é para mostrar a sutil diferença. Hb AA (1, 2, 3, 6); Hb AS (4) e Hb A + Malmo (5). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
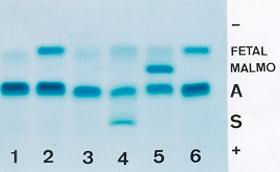
Figura 5.11 – Eletroforese em agarose ácida. A Hb Malmo separou-se da Hb A e situa-se entre esta e a Hb Fetal. Hb AA (1 e 3); Hb AF (2 e 6); Hb AS (4); Hb A + Malmo (5). Foto: Cortesia do Laboratório Santa Luzia de Florianópolis. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
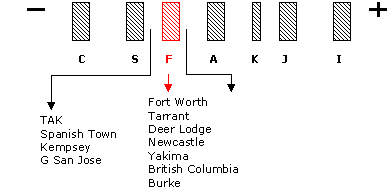
Hb Variantes similares à Hb Fetal A maioria das variantes que se posicionam como se fossem Hb Fetal, ou próximo dessa posição padrão, se devem a mutações que envolveram trocas de aminoácidos de pI diferentes, ex.: Glu ® Gli, Glu ® Asn, ou seja, se perde carga negativa de Glu ou Asp em troca de aminoácidos neutros (“sem carga”). Algumas dessas trocas ocorrem em regiões internas que podem afetar a estabilidade ou a oxigenação. A figura abaixo apresenta algumas das principais variantes na posição da Hb Fetal, ou próximo a ela. Na descrição detalhada de cada variante será apresentada sua concentração média em heterozigose. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb Fort Worth (a 27 Glu – Gli) Eletrof. ágar-ácido: similar à Hb A Eritrograma: fenótipo de talassemia menor Teste específico: concentração de Hb = 5 a 10% Característica: Hb variante com fenótipo talassêmico Hb Tarrant (a 126 Asp
– Asn) Hb Deer Lodge (b 2 His
– Arg) Eletrof. ágar-ácido: similar à Hb A Eritrograma: anemia hemolítica Teste específico: Pesquisa de Heinz: + e Instabilidade: + Característica: Hb instável e Concentração de Hb = 17% Hb Yakima (b 99 Asp
– His) Hb British Columbia (b
101 Glu – Lis) Hb Burke (b 107 Gli
– Arg) Hb Tak (inserção de aminoácidos na
C-terminal da globina alfa) Hb Spanish Town (a 27
Glu – Val) Hb Kempsey (b 99 Asp
– Asn) Hb G San Jose (b 7
Glu – Gli)
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
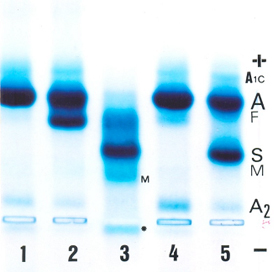
Figura 5.12 – Eletroforese alcalina de hemoglobina em gel de agarose. (1) Hb AA; (2) Hb A + G San Jose; (3) Hb SFM; (4) Hb AF + A2 aumentada; (5) Hb AS. Obs.: M: meta Hb S, o número 4 é um caso de talassemia beta menor com Hb A2: 5,6% e Hb Fetal: 4,8%. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb variantes similares à Hb S Um
representativo número de Hb variantes migra na mesma posição
que da Hb S. A maioria é diferenciada pela eletroforese ácida,
com exceção da Hb Menphis e da Hb Hasharon. Quase
todas as mutações das Hb variantes que migram na posição
da Hb S ocorreram na superfície ou região externa
da globina alfa ou beta, locais que não produzem efeitos
deletérios à molécula. Algumas outras, entretanto,
caracterizada com Hb instáveis, tem mutações
em regiões estabilizadoras (a1b1
ou a2b2)
e regiões invariantes. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
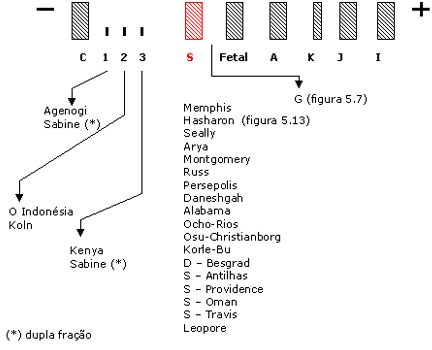
Tabela 5.3: Relação das principais hemoglobinas variantes que migram na posição de Hb S em eletroforese de pH alcalino, que são raríssimas e menos freqüente que Hb D Los Angeles.
* Duplas mutações na globina beta, além das mutações apresentadas todas tem a mutação da Hb S (b6 Glu - Val).
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb Agenogi (b 90 Glu – Lis) Eletrof. ágar-ácido: entre Hb S e Hb C Eritrograma: normal Teste específico: concentração: 40 – 45% Característica: Hb variante com alteração fisiológica Hb Sabine (b 91 Leu
– Pro) (figura 5.14) Hb O Indonésia (a
Glu – Lis) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
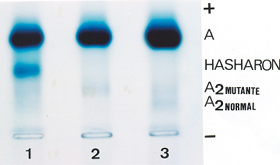
Figura 5.13 – Eletroforese alcalina de hemoglobinas em gel de agarose. (1) Hb A + Hb Hasharon, que migra na mesma posição de Hb S; (2) Hb AA; (3) Hb A com Hb A2 mutante (Hb A2 Babinga) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
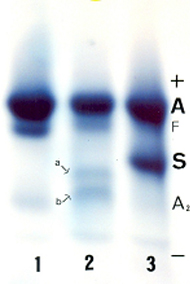
Figura 5.14 – Eletroforese alcalina de hemoglobina em acetato de celulose. (1) Hb A + Hb Fetal aumentada [12%]; (2) Hb A + Hb Sabine com duas frações a e b, e Hb Fetal aumentada [3,8%]; (3) Hb AS. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
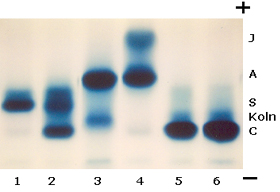
Figura 5.15 – Eletroforese alcalina de hemoglobinas em gel de agarose. (1) Hb SS; (2) Hb SC; (3) Hb A + Hb Koln; (4) Hb AJ; (5) e (6) Hb CC. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
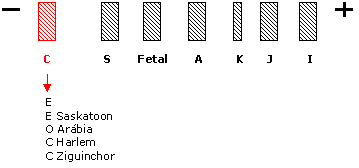
Hb variantes similares à Hb C As
Hb variantes que se posicionam na região da Hb C, com exceção
da Hb E, não causam alterações fisiopatológicas,
pois as mutações envolvem regiões externas
da molécula. O posicionamento lento dessas hemoglobinas variantes
se deve geralmente à troca de aminoácidos com cargas
negativas (Glu e Asp) por outros de cargas positivas (Arg, Lis e
His). É importante destacar que na região de Hb C
situam-se a maioria dos mutantes de globinas delta, caracterizando
as variantes de Hb A2, que serão abordadas no final deste
item. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb E (b 26 Glu – Lis) Eletrof. ágar-ácido: similar à Hb A Eritrograma: anemia microcítica Teste específico: Instabilidade: + Característica: Hb variante discretamente instável e Concentração: 20 a 25% Hb E Saskatoon (b
22 Glu – Lis) Hb O Arábia (b
121 Glu – Lis) Hb C Harlem (b 6 Glu
– Val / b 73 Asp - Asn) Hb Ziguinchor (b 6 Glu
– Val / b 58 Pro –
Arg)) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb variantes similares à Hb K As hemoglobinas variantes com posicionamento discretamente mais rápido que a Hb A são em número reduzido. É provável que esse fato se deve à dificuldade de visualização ou da detecção por procedimentos eletroforéticos e cromatográficos. A figura 5.16 mostra a Hb K em heterozigose com a Hb A (AK) e é possível observar que a dificuldade na sua identificação eletroforética se deve à sua proximidade com a Hb A. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
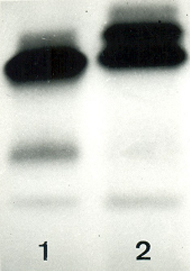
Figura 5.16 – Eletroforese alcalina de hemoglobina em acetato de celulose. (1) Hb AA com A2 aumentada – paciente com talassemia beta menor; (2) Hb A + Hb K (Hb AK). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
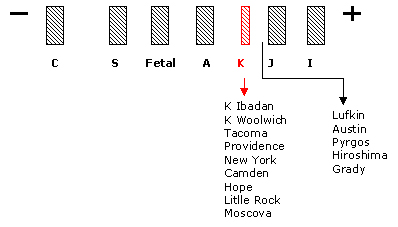
O posicionamento desse grupo de Hb variantes se deve a mutações que envolvem trocas de aminoácidos com ganho de carga negativa, por exemplo: um aminoácido neutro (Gli) é trocado por outro carregado negativamente (Glu). Entretanto a diferença de pI da molécula mutante em relação à Hb A é muito pequena e esse fato se caracteriza pela discreta mobilidade rápida da Hb variante. A figura abaixo mostra algumas variantes típicas desse fracionamento. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb K Ibadan (b 46 Glu – Glu) Eletrof. ágar-ácido: similar à Hb A Eritrograma: normal Teste específico: concentração: 45% Característica: Hb variante sem alteração funcional Hb K Woolwich (b 132
Lis – Gln) Hb Tacoma (b 30 Arg
– Ser) Hb Providence (b 82
Lis – Ans) Hb New York (b 113 Val
– Glu) Hb Camden (b 131 Gln
– Glu) Hb Hope (b 136 Gli –
Asp) Hb Little Rock (b 143
His – Gln) Hb Moscova (b 24 Gli
– Asp) Hb Lufkin (b 29 Gli
– Asp) Hb Austin (b 40 Arg
– Ser) Hb Pyrgos (b 83 Gli
– Asp) Hb Hiroshima (b 146
His – Asp) Hb Grady (a 118 –
119 inserção de Glu – Fen – Ter) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb variantes similares à J O
número de hemoglobinas variantes com mobilidade rápida
e descrita como similares à Hb J são cerca de 60 tipos.
A maioria dessas variantes se deve a mutações na globina
alfa e, por essa razão, suas concentrações
são abaixo de 25%. Esse fato decorre devido à mutação
atingir apenas um gene alfa dos quatro existentes, assim admite-se
que 25% da síntese de globina alfa esteja afetada. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
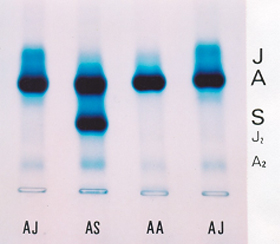
Figura 5.17 – Eletroforese alcalina de hemoglobina em gel de agarose, com o fracionamento de Hb AJ, Hb AS e Hb AA. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
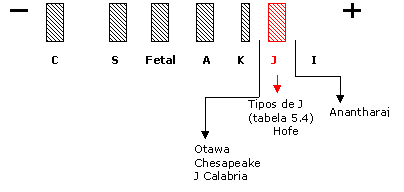
Por ser de fácil identificação as variantes que se posicionam na região de Hb J são descritas simplesmente como Hb J, destacando os locais de suas identificações: J Paris, J Oxford, etc. Mas há outras variantes que não incluem a letra J na sua identificação, conforme mostra a figura abaixo. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tabela 5.4 – Identificação de 25 variantes denominadas por Hb J selecionadas entre as 62 descritas até o presente. 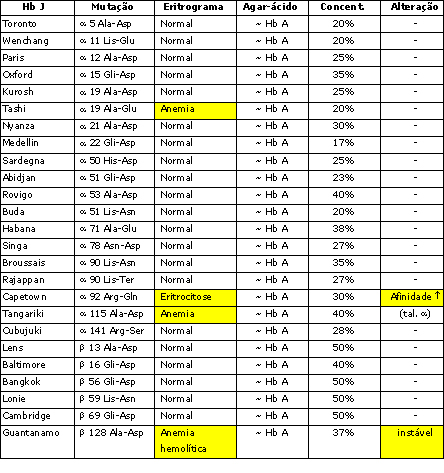 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb Hofu (b 126 Val – Glu) Eletrof. ágar-ácido: similar à Hb A Eritrograma: normal Teste específico: Instabilidade: + Característica: Hb variante instável e Concentração: 50% Hb Otawa (a 15 Gli
– Arg) Hb J Calabria (b 64
Gli – Asp) Hb Anantaraj (a 11 Lis
– Glu) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hb variantes similares à Hb
I São poucas as hemoglobinas variantes com a mobilidade rápida da Hb I. A similaridade de sua posição inclui, além de três diferentes tipos de Hb I, a Hb H (figuras 5.18 e 5.19). |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
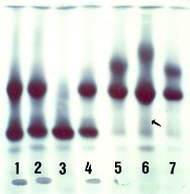
Figura 5.18 – Eletroforese alcalina, com destaque para as hemoglobinas rápidas J e I. (1), (2) e (4) Hb AC; (3) Hb CC; (5) e (7) Hb AJ; (6) Hb AI. Observar a fração I2 (aI2 dA2) formada pelo fato da Hb I ser variante de globina alfa. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
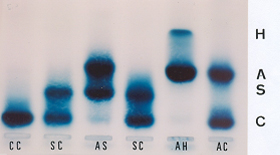
Figura 5.16 – Eletroforese alcalina de hemoglobinas em gel de agarose. Destaque para a posição da Hb H que migra na região de Hb I. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
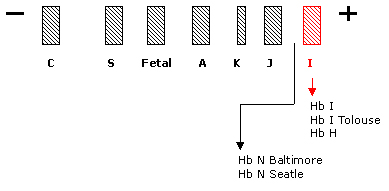
A rápida mobilidade da Hb I se deve à troca de cargas elétricas motivada por mutações que retiram aminoácidos de carga positiva (ex.: Lis) e a entrada de outros de carga negativa (ex.: Glu). Diante disso a fração se move com extrema rapidez no procedimento eletroforético. A figura abaixo representa a posição da Hb I com algumas variantes que se posicionam de forma similar e outras discretamente menos rápidas. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb I (a 16 Lis – Glu) Eletrof. ágar-ácido: similar à Hb A Eritrograma: normal Teste específico: Concentração: 25% - Hb I2 Característica: Hb variante sem alteração fisiológica Hb I Tolouse (b 66 Lis
– Glu) Hb H (b 4 – Talassemia
alfa) Hb N Seatle (b 61 Lis
– Glu) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
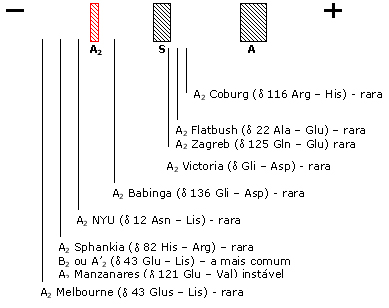
Hb variante de Hb A2 As variantes de Hb A2 se devem a mutações que ocorrem na cadeia polipeptídica da globina delta. Há cerca de 15 variantes, todas com fenótipo normal; apenas duas apresentam alterações fisiológicas de instabilidade e aumento da afinidade pelo oxigênio, sem conseqüências para seus portadores. As concentrações dessas variantes são em torno de 0,5 a 1,8%, fato que muitas vezes passam desapercebidos ao analista. Eletroforeticamente, metade dessas variantes se posicionam discretamente mais lentas que a Hb A2 normal e a outra metade um pouco mais rápido, conforme mostra a figura abaixo de dez variantes de Hb A2. A figura 5.20 mostra uma variante da Hb A2 conhecida como A2 Babinga que migra discretamente mais lenta que a Hb A2 normal. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
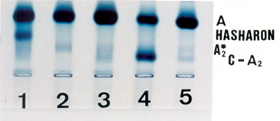
Figura 5.20 – Eletroforese alcalina de hemoglobina em gel de agarose. Da esquerda para a direita: (1) Hb A + Hasharon; (2) Hb AA; (3) e (5) Hb A + A2 Babinga; (4) Hb AC. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hb variantes de Hb Fetal As variantes
da Hb Fetal são identificadas somente no período entre
o nascimento até o sexto mês de idade, quando há
elevada concentração de Hb Fetal. Dessa forma, a quase
totalidade das identificações dessas variantes são
descritas em recém-nascidos. A figura 5.21 mostra a Hb F
Texas, uma variante muito lenta da Hb Fetal que se posiciona eletroforeticamente
atrás da Hb A2 ou da Hb C. Como é possível
notar nessa figura, o portador tinha Hb A + Hb Fetal + Hb Fetal
Texas, pois era recém-nascido. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
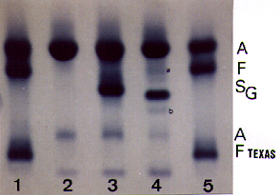
Figura 5.21 – Eletroforese de hemoglobina em agarose com pH alcalino, com destaque para a tríplice heterozigose (Hb ASG). A Hb SG* é uma forma híbrida proveniente da combinação entre aG2 e bS2. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
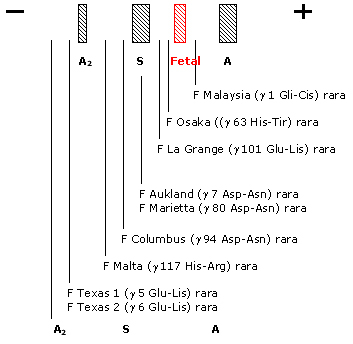
Há cerca de quarenta variantes de Hb Fetal e quase todas são eletroforeticamente mais lentas, algumas entre Hb S e Hb A2. Apenas três são mais lentas que a Hb A2: Hb F Texas 1, Hb F Texas 2 e Hb F Carlton. A figura abaixo mostra algumas dessas variantes. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||